锂-氮电池的阴极机理与锂介导的氮还原(LiNR)相似。在这里,锂-N
2、锂-NR 和铜-锂电池被合并为一个毫升规模的铜(N
2)-锂系统。利用具有锂氧化反应(LiOR)的锂阳极可确保向活性 N
2 不间断地供应锂离子。锂氧化反应不仅能提高电解质的稳定性,还能通过剥离锂离子来降低电压,这与锂氮反应通常采用的惰性铂阳极截然不同。值得注意的是,对阳极室内氨气积累的异常观察阐明了反应中间产物的存在和作用。以锂再生为目的的充电过程面临着高极化问题,因此提出了一种涉及低电流充电的循环程序,以改善循环。本研究综合了三个不同研究方向的见解,充分利用了它们各自的优势和科学见解。由于锂阳极的渐进性,锂-N
2 电池成为合成氨的一种极具优势的策略。

图1. (A) Cu(N
2)-Li电池充放电过程中锂介导氨合成的传统观点和(B)修正观点。
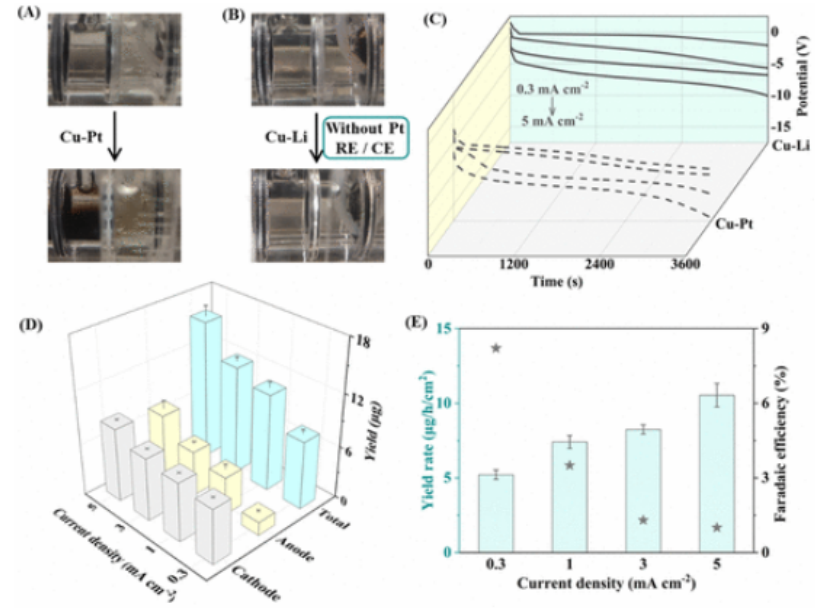
图2. (A) 铜-铂和 (B) 铜-锂的初始状态和终端状态照片。(C) 不同电流密度下的电压-时间曲线;(D) 阴极、阳极和总氨产量(带误差条);(E) Cu-Li 的氨产量和法拉第效率(带误差条)。

图3. 电解后电流密度为 (A) 0.3、(B) 1、(C) 3 和 (D) 5 mA cm
-2 的阴极的扫描电镜照片。电解后 (E) N 1s 和 (F) F 1s 的 XPS 精密光谱。

图4. 电压(E)和电荷(Q)随时间变化的曲线,循环时间限制为 600 秒。
相关研究成果由中国石油大学Hui Sun等人2024年发表在The Journal of Physical Chemistry Letters (链接:https://doi.org/10.1021/acs.jpclett.4c01328)上。原文:Cu(N
2)-Li Battery for Ammonia Synthesis
转自《石墨烯研究》公众号







